Od początku pandemii byliśmy zapewniani, że społeczne maskowanie zgodności rozwiąże nasze problemy i powstrzyma rozprzestrzenianie się SARS-CoV-2. Jednak dane z rzeczywistych aplikacji konsekwentnie pokazują, że zawodzą one jako środek łagodzący dla ochrony osobistej, i zamiast korygować kurs na przypadkowych wskazówkach, które zostały rozdane, powiedziano nam, aby maska trudniej z coraz bardziej restrykcyjnymi, aczkolwiek skutecznie niełagodzącymi aparatami.
Ale dlaczego czy zawiedli i dlaczego nadal zawodzą? Poniżej zagłębimy się w szczegóły, dlaczego nawet zakładając hipotetyczną doskonałą zdolność wychwytywania, N95 nie ograniczają rozprzestrzeniania się SARS-CoV-2.
Powinniśmy zacząć od spojrzenia na przenoszenie wirusów i produkcję materii zakaźnej jako widma, w oparciu o ciężkość choroby, odpowiedź immunologiczną danej osoby i postęp w przebiegu choroby. Wykazano, że wszystkie one mają znaczący wpływ na miano wirusa u osoby zakażonej SARS-CoV-2. Omówimy dane wyjściowe w porównaniu ze wskaźnikami zakaźności oraz metody pomiaru minimalnej dawki zakaźnej.
Są to ważne czynniki, które należy wziąć pod uwagę w łagodzeniu patogenów, nawet niezależnie, ale połączone, mogą nam konkretnie pokazać, czy dane podejście przyniesie pożądany wynik w eliminacji zagrożenia zakaźnego. Dane wyjściowe emisji z dróg oddechowych pokazują, ile materii jest wydalane przez osobę i czy są one przenoszone z patogenem układu oddechowego, ale dane wyjściowe różnią się znacznie w zależności od cięższych stadiów początku choroby, okresów rekonwalescencji i kiedy wynik PCR-ujemny dla danego patogenu.
Porównując wydajność ze stosunkiem cząstek do jednostek tworzących płytkę (PFU), otrzymujemy wskaźnik liczby emitowanych cząstek, które są zdolnymi do życia wirionami zdolnymi do wywołania infekcji. Każda z tych jednostek zakaźnych jest określana jako PFU. Liczba PFU, które potencjalny gospodarz musi otrzymać, jest podawana jako minimalna dawka zakaźna (MID), która jest progiem, po osiągnięciu którego należy spodziewać się wystąpienia zakażenia.
Patrząc na liczby dotyczące stosunku cząstek do PFU i obliczając potencjał MID, produktem końcowym jest potencjalna liczba osób, które mogą zostać zakażone w danym okresie czasu.
Z tym progiem MID dla potencjalnej infekcyjności, możemy następnie zastosować hipotetyczną doskonałą zdolność wychwytywania danej aparatury, aby sprawdzić, czy w najlepszym scenariuszu prawdopodobieństwo złagodzenia przez aparaturę lub zapobieżenia osiągnięciu progu MID dla zagrożenia.
Tutaj patrzymy na wydajność, stosunek cząstek do PFU i MID dla SARS-CoV-2 w porównaniu z hipotetyczną doskonałą zdolnością wychwytywania dla N95, aby wykazać, że nawet przy doskonałym wskaźniku wychwytywania (w tym przypadku materia znacznie mniejsza niż urządzenie jest zatwierdzone lub zaprojektowane do wychwytywania), 5% procent nigdy nie wychwytywanych to wciąż wystarczająco duże potencjalne narażenie na materię zakaźną, aby spowodować infekcję.
Zasięgi cząstek i odpowiadające im zachowanie emitowanej materii
Środki łagodzące pandemię należało rozpocząć od minimalnej wielkości cząstek, która w przypadku SARS-CoV-2 wynosi 0.06-0.14 µm. Chociaż często naciskane przez urzędników zdrowia publicznego, N95 są oceniane i zatwierdzane wyłącznie do wychwytywania materii większej niż 0.3 µm. Wykazano, że spada ponad 90% procent wydychanych cząstek dla 0.3 µm. Materia tego rozmiaru pozostaje w powietrzu przez dłuższy czas — godziny, a nawet dni, w zależności od kursów wymiany powietrza w danej przestrzeni. Wykazano, że SARS-CoV-2 pozostaje żywy po godzinach w postaci aerozolu na zewnątrz żywiciela i przez kilka dni na powierzchniach.
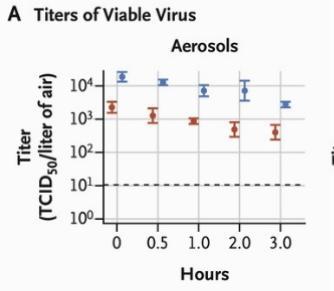
"SARS-CoV-2 zaobserwowano obecność wirusa żywotne przez 3 godz. w aerozolach, przy spadku stężenia wirusa zakaźnego od 103.5 do 102.7 TCID50 za litr powietrza”.
W badaniu tym wykorzystano laboratoryjnie wygenerowane aerozole zawierające zakaźny SARS-CoV-2 i zaobserwowano żywotność emitowanej materii na różnych powierzchniach oraz w postaci aerozoli w czasie.
Rozważając następujące kwestie, można się również zastanawiać, czy porowata maska i membrany respiratora odegrały rolę w zwiększeniu okresu żywotności materii wirusowej:
"Czasy przetrwania wirusów przenoszonych drogą powietrzną na powierzchniach różnią się na podstawie czy powierzchnie są nieporowate (np. plastik, stal nierdzewna, szkło) czy porowate (np. papiery i ubrania). Nieporowate powierzchnie są głównymi czynnikami przenoszenia chorób, ponieważ zaobserwowano, że czas przeżycia wirusów przenoszonych drogą powietrzną na nich jest znacznie dłuższy niż na powierzchniach porowatych”.
Maski i maski oddechowe z pewnością zaliczają się do porowatych powierzchni. Wiele respiratorów jest również zbudowanych z rozdmuchiwanych ze stopu tworzyw sztucznych. Czy żywotność wirusów na błonach masek została zbadana w wystarczającym stopniu?
Wskaźniki żywotności aerozoli są ważne, ponieważ pokazują zdolność przenoszenia w zamkniętych przestrzeniach bez obecności osoby zdolnej do przenoszenia. Z zakaźny osobnik obecny i emitujący w danej przestrzeni, produkcja byłaby stała, a żywotna materia wirusowa zwiększałaby nasycenie atmosfery patogenem na podstawie jednego oddechu.
Przeoczanym, ale krytycznym problemem związanym z maskami i respiratorami jest uszczelnienie – małe szczeliny sprawiają, że te aparaty są nieskuteczne dla użytkownika. Rzadko, jeśli w ogóle, ktoś nosi te aparaty prawidłowo, zgodnie z niezbędnymi warunkami noszenia, więc spotykamy się z nieprawidłowym noszeniem już niełagodzących aparatów.
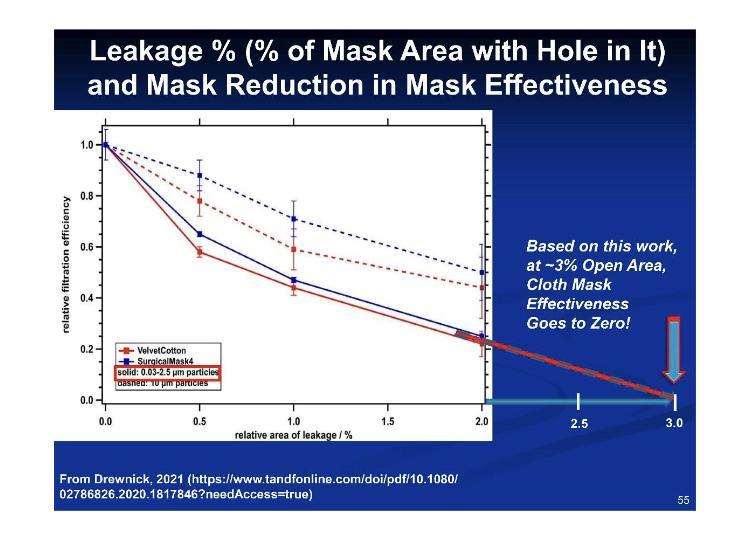
Zgodnie z tymi liczbami dotyczącymi dopasowania w stosunku do wycieku, 3.2% wycieku odpowiada 100% nieskuteczności.
Są to wszystkie czynniki, które należy wziąć pod uwagę przy usuwaniu przyczyny, dla której urządzenie nie łagodzi danego zagrożenia. Następnie badając emisje, minimalną dawkę zakaźną, jednostki tworzące płytkę nazębną i ich powiązania, możemy lepiej zrozumieć, dlaczego kontrole inżynieryjne były zawsze właściwą reakcją, a nie masowe wdrażanie aparatów do ochrony dróg oddechowych.
Emisje oddechowe „chorych” pacjentów – wyniki testu PCR-pozytywne i negatywne:
W badaniach nad wytwarzaniem aerozolu u osób zdrowych i SARS-CoV-2 z pozytywnym wynikiem PCR, ponad 90% procent cząstek emitowanych przez osoby z pozytywnym wynikiem PCR miało wielkość poniżej 0.3 µm, a zliczenia wyemitowanej materii przeprowadzono porównując osoby z różnym stopniem choroby z osobnikami z ujemnym wynikiem PCR.
"Mediana wypuściła powietrze liczba cząstek była znacznie podwyższona u pacjentów SARS-CoV-2 z pozytywnym wynikiem PCR (1490.5/l [46.0–34,772.0 252.0/l]) w porównaniu ze zdrowymi kontrolami (0.0/l [882.0–0.0001/l]; p < XNUMX”.
Jeśli użyjemy wskaźnika emisji z dróg oddechowych 4.3-29 litrów na minutę (z podręcznika EPA Exposure Factors Handbook), najwyższy zakres pozytywnych reakcji PCR wynoszący 34,772 29 cząstek na litr pomnożony przez 1,008,388 litrów na minutę wynosi aż XNUMX XNUMX XNUMX cząstek emitowanych na minutę .
Chociaż nie twierdzę, że wszystkie te cząsteczki były pojedynczymi cząsteczkami wirusa lub żywotnymi cząsteczkami wirusa, to jednak istnieje bardzo znacząca różnica w materii emitowanej przez osobniki pozytywne i negatywne pod względem PCR (mediana wartości 1,490.5 vs 252). Po omówieniu roli PFU zostanie wprowadzony współczynnik konwersji cząstek na PFU.
Rozmiary cząstek i wskaźniki emisji:
W badaniu wcześniej omawiano zakresy wielkości emitowanych cząstek u osób z dodatnim i ujemnym wynikiem SARS-CoV-2.
"Odnośnie cząstki rozkład wielkości, dostępne kanały wielkości (w sumie 14 kanałów wielkości od 0.15 do 5.0 μm) analizowano w trzech pasmach wielkości: <0.3 μm, 0.3–0.5 μm i > 0.5–5.0 μm. W obu grupach większość aerozoli (>90% w grupie dodatniej pod względem SARS-CoV-2 PCR i >78% w grupie -ujemnej) znajdowała się w najmniejszym zakresie (<0.3 μm). Szczególnie w przypadku grupy zakażonej COVID wzrost całkowitego stężenia aerozolu był zdominowany przez wzrost cząstek ≤0.3 μm”.
Dziesięć osób z 64 hospitalizowanych pacjentów, z których pobrano próbki, które były jednymi z najcięższych przypadków, było odpowiedzialnych za około 64.8% procent liczby cząstek wydychanych, dlatego ważne jest, aby w tym przypadku przyjrzeć się najmniej konserwatywnego zakresu wyjściowego i potencjalnej zakaźności podczas przeprowadzania obliczeń wyjściowych i minimalnej dawki zakaźnej. W szczególności w gazecie stwierdzono:
"W SARS-CoV-2 Grupa z pozytywnym wynikiem PCR, 15.6% (n = 10/64), wykazywała wysokie zliczenia i była odpowiedzialna za 64.8% wszystkich zliczeń cząstek wydychanych w grupie. Co więcej, 15.6%, co odpowiada 3.5% wszystkich pacjentów (n = 10/288), było odpowiedzialne za 51.2% wszystkich wydychanych cząstek”.
Jeśli porównamy osoby doświadczające największego nasilenia choroby ze wskaźnikami zakaźności, możemy dowiedzieć się więcej o wydalaniu żywotnych cząstek przez osoby zakaźne. Biorąc pod uwagę niską wydajność zarówno emitowanej materii, jak i wirionów przez osoby testowane z negatywnym wynikiem PCR i odzyskujące pozytywny wynik testu PCR, można bezpiecznie spekulować, że mówi to o niskim prawdopodobieństwie bezobjawowej transmisji będącej głównym czynnikiem rozprzestrzeniania się wirusa.
Obecność kopii RNA a koncentracja żywotnych wirionów
Nie wszystkie kopie RNA lub cząsteczki wirusa są zdolne do tworzenia PFU powodujących replikację wirusa. Chociaż podano dane dotyczące liczby generowanych jednostek zakaźnych, tak jest nie współczynnik emisji. Są to szacunki dotyczące całkowitej produkcji wirusa podczas infekcji.
"Dzielenie przez szacunki dla odwrotności wskaźnika klirensu wirusa daje szacunkową całkowitą produkcję 3 × 109 do 3 × 1012 wirionów lub 3 × 105 do 3 × 108 jednostek zakaźnych w ciągu całego przebiegu charakterystycznej infekcji”.
W uproszczeniu oznacza to całkowitą produkcję od 3 miliardów do 3 bilionów cząsteczek wirusa lub od 300,000 300 do XNUMX milionów jednostek zakaźnych generowanych w trakcie choroby.
Wyjście wirionów
Istnieją różne metody ustalania produkcji wirionów, które dają nieco inne zakresy, patrząc obok siebie. Niektóre badania wskazują na całkowitą emisję wirionów, na przykład:
"Niektórzy pacjenci mają miana wirusa, które przekraczają średnie miano Wölfela i wsp. o ponad dwa rzędy wielkości, zwiększając w ten sposób liczbę wirionów w emitowanych kropelkach do znacznie ponad 100,000 XNUMX na minutę mówienia”.
Inne badania podają całkowitą liczbę cząstek i polegają na zastosowaniu współczynników konwersji z całkowitej produkcji na zdolne do życia wiriony. Należy ustalić, że całkowita ilość cząstek wirusa nie jest równa całkowitej liczbie żywotnych wirionów, czyli wirionów zdolnych do tworzenia jednostek tworzących łysinki (PFU).
PFU – Zrozumienie cząsteczek wirusa potrzebnych do utworzenia poszczególnych jednostek tworzących płytkę nazębną (PFU):
Chociaż wszystkie emitowane wirusowe RNA i cząsteczki wirusa nie są zdolne do replikacji wirusa i tworzenia PFU, rozumie się, że każdy PFU jest tworzony przez jedną żywotną cząsteczkę wirusa. Poniższe fragmenty omawiają wpływ PFU na infekcje wirusowe i ich początek.
"Test jest zaprojektowany tak, że każda łysinka jest wynikiem infekcji poprzez namnażanie pojedynczej zakaźnej cząsteczki wirusa. W związku z tym PFU/ml uważa się za miarę liczby jednostek zakaźnych na mililitr (j.m./ml), z zastrzeżeniem, że nie można być pewnym stosunku jeden do jednego łysinek do cząstek zakaźnych w zastosowanej porcji. ”
"Dla większości wirusów zwierzęcych, jedna zakaźna cząsteczka wystarczy, aby zainicjować infekcję”.
"Charakter liniowy krzywej dawka-odpowiedź wskazuje, że pojedynczy wirion jest zdolny do zainicjowania infekcji. Jednak wysoki stosunek cząstek do pfu wielu wirusów pokazuje, że nie wszystkie wiriony odnoszą sukces. Wysoki stosunek cząstek do pfu jest czasami spowodowany obecnością niezakaźnych cząstek z genomami, które zawierają śmiertelne mutacje lub które zostały uszkodzone podczas wzrostu lub oczyszczania”.
"Ogólnie się przyjmuje że płytka jest wynikiem zakażenia komórki pojedynczym wirionem. Jeśli tak jest, to wszystkie wirusy wytworzone z wirusa w płytce powinny być klonami, innymi słowy powinny być genetycznie identyczne”.

Podsumowując, jedna żywotna cząsteczka wirusa lub wirion jest w stanie wytworzyć jedną PFU, w której ta wirusowa cząsteczka replikuje się. Część utworzonej materii to wyłącznie wirusowe RNA niezdolne do niezależnego powodowania infekcji, a część utworzonej materii jest zdolna do replikacji i infekcji.
Związek pomiędzy całkowita produkcja cząstek i tworzenie PFU nazywane jest stosunkiem cząstek do PFU. W przypadku SARS-CoV-2 stosunek emitowanych cząstek do PFU wynosi od 1000 do 1,000,000 XNUMX XNUMX.
Badania PFU i minimalnej dawki zakaźnej
Nasze tempo oddychania zmienia się w zależności od wieku i poziomu aktywności. Średnia częstość oddechów człowieka wynosi 16-20 oddechów na minutę. Do celów tej dyskusji zostanie zastosowana szybkość oddychania 4.3-29 litrów na minutę (z podręcznika EPA Exposure Factors Handbook). To odniesienie daje zakres aż 53 litrów na minutę. Przyjrzymy się produktowi jako wirionom na minutę i minimalnej dawce zakaźnej jako PFU i wirionom do przenoszenia, ponieważ oba są badane w dostępnych badaniach.
Minimalna dawka zakaźna (MID) Dane z literatury:
Badania porównawcze różnych wirusów układu oddechowego i badania na zwierzętach SARS-CoV-2 zostały wykorzystane do wielu szacunków MID, ale niniejszy artykuł skupia się w jak największym stopniu wyłącznie na badaniach na ludziach.
"Chociaż MID SARS-CoV-2 u ludzi potrzebuje więcej badań, oczekuje się, że będzie to około 100 cząsteczek wirusa. Jedyne badanie na ludziach dotyczące koronawirusa zostało zgłoszone dla HCoV-229E, a jego MID wynosi 9 PFU. Co więcej, jeśli transmisja aerozolu jest dominującym trybem, MID byłby niższy”.
"W rzeczywistości, infekcje na bazie aerozolu wymagają mniejszych dawek, np. ~100 razy mniej niż infekcje kropelkowe”.
"Minimalna dawka zakaźna SARS-CoV-2 powodującego COVID-19 u ludzi w ocenianych badaniach przekrojowych i seriach przypadków była niska; w badaniu serii przypadków, w którym zbadano dawkę zakaźną w 273 próbkach od 15 pacjentów SARS-CoV-2-dodatnich, wykryto minimalną dawkę zakaźną 1.26 PFU in vitro w teście COVID-19-RdRp/Hel.1 W innym badaniu, 248 Oceniono próbki ustno-nosowo-gardłowe osób z COVID-19 i zgłoszono, że dawka zakaźna wynosiła 364 PFU”.
"W badaniu serii przypadków w którym oceniono 97 dzieci w wieku 10 lat i młodszych, 78 dzieci w wieku 11–17 lat i 130 dorosłych, dawka zakaźna u dzieci w wieku 11–17 lat była niższa niż w dwóch pozostałych grupach (125 PFU). Dzieci miały niższy wzrost żywego wirusa, wyższe progi cyklu i niższe stężenie wirusa w porównaniu z dorosłymi, więc dzieci nie są głównymi nosicielami infekcji. Dzieci w wieku ⩽10 lat częściej niż inne były bezobjawowe”.
"Jeden z najbardziej dobrze omówione (sic) jest badanie przeprowadzone przez Basu i wsp., którego głównym celem była ocena wielkości kropelek, które mają wysokie prawdopodobieństwo wywołania infekcji. Ale poza tym odkryciem mieli również pewne punkty związane z wiremią, która może powodować infekcję. Odkryli, że liczba wirionów umieszczanych w blisko położonej nosogardzieli osobnika w ciągu 2.5 godziny wynosi w przybliżeniu (11/5) wirionów na minutę × 60 min × 2.5 h = 330”.
Badania porównawcze obejmujące inne koronawirusy wykazały, że PFU mogą być dość niskie w przypadku wirusów układu oddechowego.
"Szacowana zakaźność SARS-CoV-1 był porównywalny z innymi koronawirusami, w tym HCoV-229E, czynnikiem sprawczym łagodnego przeziębienia u ludzi. ID10 i ID50 SARS-CoV-1 zostały zgłoszone jako 43 i 280 PFU (400 TCID50) w badaniu eksperymentalnym”.
"Identyfikator człowieka50 dla sezonowego koronawirusa podtypu 229E, który powoduje łagodne przeziębienie u ludzi, wyniósł 13 TCID50".
Liczby omówione w dostarczonych badaniach dotyczących SARS-CoV-2 wynosiły 1.26, 100, 125, 330 i 363 PFU do transmisji, ponownie mówiąc o szerokim spektrum podatności.
Produkcja żywotnych wirionów a potencjał progowy minimalnej dawki zakaźnej
Korzystając z tych dostępnych danych, możemy zmierzyć się z twierdzeniem, że N95 zapewniają znaczącą wartość ochronną przed zakaźnymi aerozolami, patrząc na wkład wyjściowy, potencjał zakaźny emitowanej materii wirusowej, zakresy PFU, a następnie możemy porównać te zakresy z hipotetyczną doskonałą zdolnością wychwytywania N95 przechwytywanie 95% procent materii, w porównaniu z pozostałymi nieprzechwyconymi 5% procent. Ponownie zauważ, że N95 nie są zaprojektowane ani zatwierdzone do wychwytywania <0.3 µm, a my omawiamy patogen, który ma minimalną wielkość żywotnych cząstek 0.06-0.14 µm.
Emisje oddechowe Wykazano, że od osoby zakaźnej osiągają ponad 100,000 750,000 wirionów w ciągu jednej minuty, chociaż nie można założyć, że wszystkie emitowane wiriony są zakaźne. Dodatkowe prace badawcze twierdzą, że wydajność sięga XNUMX XNUMX wirionów na minutę (ale brakuje danych potwierdzających takie twierdzenia). Należy również zauważyć, że oczywiście nie wdychamy całej wydychanej materii danej osoby, ale nasza bliskość do osoby zdolnej do przenoszenia, tempo jej wydalania, czas przebywania w danej przestrzeni i wentylacja w danej przestrzeni są czynnikami, które będą miały wpływ na prawdopodobieństwo transmisji, którego nie można wyrazić w sposób liniowy lub przewidywalny.
W badaniu zbadaliśmy powyżej, najwyższy wyjściowy zakres PCR-dodatni wynosił 34,772 64 cząstek na litr, przy czym te emitujące najwyższe zakresy wyjściowe stanowiły XNUMX% procent całkowitej emitowanej materii.
Najpierw stworzymy godzinową wydajność każdego z tych zakresów, a następnie zastosować stosunek cząstek stałych do PFU dla każdego zakresu od 1,000 1,000,000 do XNUMX XNUMX XNUMX.
Zakres wyjściowy
Godzina zakaźnego osobnika w zamkniętej przestrzeni, emitującej 100,000 6 wirionów na minutę, byłaby wynikiem 100,000 milionów wirionów (60 8 × 48 minut). 100,000-godzinny okres w zamkniętej przestrzeni równa się wyemitowaniu 480 milionów wirionów (1,000 1,000,000 x 6,000 minut). Przy stosunku cząstek do PFU wynoszącym od 48,000 do 8 XNUMX XNUMX, daje to nam XNUMX żywotnych wirionów w ciągu jednej godziny, XNUMX XNUMX w ciągu XNUMX godzin.
Podane liczby PFU z omawianych badań to 1.26, 100, 125, 330 i 363 PFU wymagane jako minimalna dawka zakaźna. Podzieliłem każdą liczbę żywotnych wirionów przez każdą liczbę PFU, aby uzyskać każdy potencjał dla wymienionego progu MID.
Zakres wyjściowy B
W badaniu zbierania cząstek dodatnich PCR, 34,772 64 cząstek na litr było najwyższym zebranym zakresem, przy około 10% procent wszystkich emitowanych i liczonych cząstek pochodzących z 2 źródeł, które były jednymi z najbardziej dotkniętych infekcją SARS-CoV-34,772 . Jeśli spojrzymy na 29 1,008,388 cząstek pomnożonych przez wielkość emisji XNUMX litrów na minutę, zakres wyjściowy wynosi aż XNUMX XNUMX XNUMX cząstek emitowanych na minutę.
Podręcznik narażenia EPA podaje zakres na minutę sięgający 53 litrów na minutę, więc użycie liczby 29 litrów na minutę nie jest najwyższym możliwym zakresem wydajności. Zastosowane zostaną zakresy wydajności 7 i 29 litrów na minutę, ponieważ są to zakresy wydajności mieszczące się w zakresach poziomu aktywności siedzącej i umiarkowanej.
Przy 29 litrach na minutę, pomnożonych przez 34,772 1,008,388 cząstek na litr (60 60,503,280 1,008,388 cząstek), przy 60-minutowym czasie produkcji produkt wynosi 484,026,240 8 1,008,388 (480 XNUMX XNUMX × XNUMX) cząstek na godzinę i XNUMX XNUMX XNUMX na okres XNUMX godzin (XNUMX XNUMX XNUMX × XNUMX minuty).
Przy stosunku cząstek do PFU wynoszącym od 1,000 1,000,000 do 60,503 484,026 8 w przypadku COVID, daje to nam XNUMX XNUMX zdolnych do życia wirionów emitowanych na godzinę i XNUMX XNUMX zdolnych do życia wirionów na okres XNUMX godzin.
Obliczenia te dają nam potencjał wyjściowy osoby zakaźnej pod względem nie tylko liczby emitowanych cząstek wirusa, ale także potencjału osiągnięcia progu MID w celu zainfekowania określonej liczby osób, na podstawie której używana jest liczba PFU.
Chociaż zakres PFU wykazany dla SARS-CoV-2 jest dość szeroki, powinniśmy przewidzieć spektrum przenoszenia w oparciu o indywidualny stan zdrowia i odpowiedź immunologiczną. Chociaż 1.26 PFU wydaje się dość niskie, wykazano, że PFU dla SARS-Cov-1 wynosi zaledwie 13 PFU, aby osiągnąć próg MID dla początku infekcji.
Nawet jeśli stosuje się niższą emisję wynoszącą 7 litrów na minutę, daje to szybkość 243,404 34,772 cząstek na minutę (7 14,694,240 x 234,404)), 60 116,833,920 243,404 cząstek na godzinę (480 8 x 1,000) i 1,000,000 1 14,604 (116,833 8 x XNUMX) cząstek na XNUMX - okres godzinowy. Przy stosunku cząstek do PFU wynoszącym od XNUMX XNUMX do XNUMX XNUMX XNUMX, XNUMX-godzinny okres daje wynik XNUMX XNUMX żywotnych wirionów i XNUMX XNUMX w okresie XNUMX-godzinnym.

Przy tych zakresach wyjściowych od siedzącego do umiarkowanego natężenia, wiele razy próg MID jest osiągany dla wszystkich ustalonych wartości PFU.
Dlaczego N95 zawiodły / zawodzą / zawiodą
Respiratory z oceną N95 są zaprojektowane i zatwierdzone do wychwytywania 95% procent materii nieolejowej o wielkości większej niż 0.3 µm. SARS-CoV-2 ma minimalny rozmiar żywotnych cząstek 0.06-0.14 µm, znacznie poniżej progu 0.3 µm, nawet jeśli jest związany z większą materią, więc jest to hipoteza o doskonałej zdolności wychwytywania dla zakresu cząstek, którego te aparaty nie są zaprojektowane lub zatwierdzone do przechwytywania, ani dane ich aplikacji nie wykazały, że działają na poziomie 95% lub w pobliżu.
Na potrzeby ćwiczenia hipotetycznej idealnej zdolności przechwytywania, przyjmiemy założenie idealnego 95% wskaźnika przechwytywania. Jeśli zastosujemy 5% wartości MID wykazanych w do wykazanych w zakresach wyjściowych A i B, zademonstruje to zakaźność żywotnych wirionów w porównaniu z 5% procentami nigdy nie wychwyconymi (np. schwytanie jest spełnione.
Zakres wyjściowy
Zakres wyjściowy B
29 litrów na minutę
7 litrów na minutę
Jeśli założymy hipotetyczną idealną zdolność wychwytywania dla N95 cząstek o zakresie wielkości cząstek, do których wychwytywania te aparaty nie zostały zaprojektowane lub zatwierdzone, i zastosujemy pozostałe 5% nigdy nie wychwytywanych, zdecydowana większość zakresów mocy wyjściowej w porównaniu z PFU wymaganych do spełnienia wymagań MID nadal pozwalają na ekspozycję na wielokrotność progu MID dla potencjalnej infekcji wielu osobników w okresach 1-godzinnych i 8-godzinnych dla każdego ustalonego zakresu produkcji.
Podsumowanie
Podczas wybuchu SARS-CoV-2 poluzowaliśmy nasze standardy łagodzenia, ponieważ ten patogen nie jest śmiertelny dla przeważającej większości ludzi, a wskaźnik przeżywalności wynosi około 99.8%. Ta nonszalancja w stosunku do reakcji specyficznej dla zagrożenia jest niezwykle niebezpieczna, gdy stosuje się ją do bardziej śmiercionośnych patogenów i elementów narażenia.
Analizując hipotetyczny najlepszy scenariusz, możemy lepiej przewidzieć, czy dany środek będzie miał łagodzący wpływ na zidentyfikowane zagrożenie. W przypadku N95 w porównaniu do mocy wyjściowej, stosunku cząstek do PFU i MID dla SARS-CoV-2, najlepszy scenariusz hipotetycznego doskonałego wychwytywania materii, do którego wychwytywania te aparaty nie są ani zaprojektowane, ani zatwierdzone, pokazuje, że nadal nie są one łagodzące dla tego zagrożenia, a zalecenia dotyczące ich stosowania należy natychmiast ponownie rozważyć.
Dodatkowe zasoby:
Omawia średnie miano wirusa z próbek: https://www.nature.com/articles/s41586-020-2196-x.
Minimalna dawka zakaźna
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7090536/ (ogólnie w MID, nie w odniesieniu do SARS-CoV-2).
Słownik
aerozol – cząsteczki rozproszone w powietrzu lub gazie, zdefiniowane jako mniejsze niż 5 mikronów.
bezobjawowy (rozprzestrzenianie się) – teoretyczna koncepcja przenoszenia patogenu na inne osoby bez wykazywania jakichkolwiek ustalonych objawów tego patogenu.
nasycenie atmosferyczne – ilość żywej materii, która pozostaje w powietrzu w zamkniętej przestrzeni.
emisje – wydychana materia oddechowa.
reżim przepływu laminarnego – cząstki płynu podążające gładkimi ścieżkami w warstwach.
minimalna dawka zakaźna – minimalna wielkość zagrożenia, na które trzeba być narażonym, aby można było przewidzieć początek choroby.
N95 - respirator z filtrem cząstek stałych, który nie wychwytuje oleju i może blokować do 95% materii o wielkości powyżej 0.3 µm.
początek – początek choroby rozpoczynającej się po osiągnięciu progu minimalnej dawki zakaźnej.
wyjście - emisje uwalniane do danego środowiska przez osobę zakaźną.
wyjście jako stała – osoba znajdująca się w zamkniętej przestrzeni, emitująca zakaźne aerozole oddechowe do danej atmosfery, nasycając tę atmosferę bardziej zakaźną materią z każdym oddechem.
stosunek cząstek stałych do PFU – współczynnik do obliczeń produkcji patogenów, który waży całkowitą liczbę emitowanych cząstek w porównaniu z cząstkami, które są żywotnie zakaźne.
PCR-ujemny – dana osoba testowana nie otrzymuje pozytywnego wyniku testu przy użyciu metodologii PCR dla danego patogenu. PCR oznacza użycie techniki reakcji łańcuchowej polimerazy.
PCR-dodatni – dany podmiot testowy otrzymuje pozytywny wynik testu, gdy jest testowany przy użyciu techniki reakcji łańcuchowej polimerazy dla danego patogenu.
doskonała zdolność przechwytywania – wychwytywanie substancji niebezpiecznych przy dopasowanej skuteczności procentowej podanej przez produkt jako hipotetycznie najlepszej możliwej szybkości.
Jednostki tworzące płytkę nazębną (PFU) – do powstania PFU potrzebny jest jeden wirion, który zakaża komórkę gospodarza, gdzie rozpoczyna się replikacja wirusa. Do wystąpienia choroby wymagany jest próg określonej liczby PFU, znany jako minimalna dawka zakaźna.
kopie RNA – materiał genetyczny wymagany do tworzenia kopii białek w komórce. Kopie RNA nie są równoznaczne z żywymi wirionami zdolnymi do replikacji.
TCID50 – skrót oznaczający dawkę zakaźną hodowli tkankowej, która jest rozcieńczeniem wirusa wymaganym do zainfekowania 50% komórek w teście hodowlanym.
miano wirusa – ilość cząsteczek wirusa w danej substancji, emisji lub w ciele osoby zakaźnej.
żywotność wirusów – wiriony zdolne do infekowania komórki i tworzenia jednostek tworzących płytki (PFU).
wirion lub żywy wirion- kompletna zakaźna cząsteczka wirusa.
Opublikowane pod a Creative Commons Uznanie autorstwa 4.0 Licencja międzynarodowa
W przypadku przedruków ustaw link kanoniczny z powrotem na oryginał Instytut Brownstone Artykuł i autor.









