Telegraph niedawno poinformowało, że powiedziano społeczeństwu, aby zaprzestało przyjmowania leków na kaszel i przeziębienie z powodu obaw związanych z bezpieczeństwem leku, folkodyny, opioidowego środka przeciwkaszlowego.
Dwadzieścia popularnych leków na kaszel i przeziębienie, w tym kapsułki Day and Night Nurse, zostało pilnie wycofanych z rynku na polecenie regulatorów leków z powodu obaw o „bardzo rzadkie” ryzyko anafilaksji, zagrażającego życiu zdarzenia niepożądanego.
Ogłoszenie „Wycofanie leków klasy 2” zaczerpnięte z rządu Wielkiej Brytanii , pokazano poniżej.

Jeśli chodzi o szczepionki mRNA COVID-19, podwójne standardy regulacyjne nigdy nie były tak rażąco oczywiste.
Anafilaksja została uznana za istotne zagrożenie przez Europejską Agencję Leków już w grudniu 2020 r. w CHMP EMA (Komitet ds. Produktów Leczniczych Stosowanych u Ludzi) Sprawozdanie z oceny na temat szczepionki Pfizer-BioNTech COVID-19, widocznej poniżej.
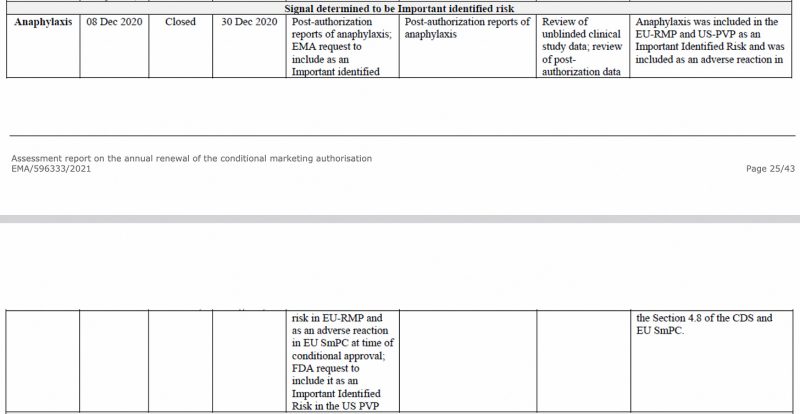
Również w pierwszej unijnej okresowej aktualizacji bezpieczeństwa Zgłoś, które posiadam wcześniej analizowaneanafilaksja została ponownie oznaczona jako ważne zidentyfikowane ryzyko.

W tym raporcie z nadzoru nad bezpieczeństwem farmakoterapii zidentyfikowano 3,827 XNUMX odpowiednich przypadków (osobników) na podstawie danych po wydaniu pozwolenia. Krajem o najwyższej zachorowalności była Japonia, a następnie Stany Zjednoczone i Wielka Brytania.
Największą liczbę zgłoszonych przypadków odnotowano wśród kobiet, szokujące 3,182 przypadki w porównaniu do 454 przypadków w przypadku mężczyzn, przy medianie wieku 44 lat. Fakt, że kobiety zgłoszono 7 razy więcej przypadków, nie jest niczym nowym. W grudniu 2021 r. I analizowane firma Pfizer przygotowała dokument dla FDA, obejmujący okres 3 miesięcy, od grudnia 2020 r. do 28 lutego 2021 r. – w przypadku anafilaksji – kobiety były 8 razy bardziej dotknięte.
Tak więc 98 procent odpowiednich zdarzeń niepożądanych (w tym reakcja anafilaktyczna, wstrząs anafilaktyczny, reakcja anafilaktoidalna i wstrząs anafilaktoidalny) zostało sklasyfikowanych jako poważne!
Ponadto w przypadku 92 procent zdarzeń czas, jaki upłynął do wystąpienia zdarzenia niepożądanego po podaniu szczepionki, wynosił mniej niż 24 godziny.

Fatalne wyniki
Spośród 3,922 zdarzeń 28 było śmiertelnych, a dla oszałamiającej liczby 704 wynik był nieznany. Nie podano numerów przypadków śmiertelnych.

Przypadki według grup wiekowych
Spośród 3,827 odpowiednich przypadków (osób), 23 pochodziło z grupy wiekowej pediatrycznej, a 3,021 z grupy wiekowej dorosłych.
Obecność chorób współistniejących
Warto zauważyć, że wystąpiło około 2/3 wszystkich przypadków anafilaksji nie mieć jakiekolwiek choroby współistniejące (problemy zdrowotne).

Biorąc pod uwagę to, co wydarzyło się od czasu wprowadzenia na rynek szczepionek mRNA COVID-19, nie jest niespodzianką, gdy czytamy: „nie zidentyfikowano żadnych nowych informacji dotyczących bezpieczeństwa dotyczące ryzyka anafilaksji po BNT162b2” (szczepionka Pfizer-BioNTech COVID-19). Podany powód (lub wymówka, za którą się ukrywają) jest taki, że „zagrożenie jest przekazywane… co obejmuje informacje o odpowiednich działaniach, które należy podjąć, w następujący sposób: „Podobnie jak w przypadku wszystkich szczepionek do wstrzykiwań, odpowiednie leczenie i nadzór muszą być zawsze łatwo dostępne w przypadku rzadkiego zdarzenia anafilaktycznego po podaniu szczepionki.”
Pod Reguła 174, Informacje dla pracowników służby zdrowia w Wielkiej Brytanii, ostatnio zmienionego w grudniu 2021 r., stwierdza się, co następuje:

n właściwie, na samym pierwszy dzień wprowadzenia szczepionki Pfizer-BioNTech COVID-19 w Wielkiej Brytanii, zgłoszono dwa przypadki anafilaksji i jeden przypadek możliwej reakcji alergicznej. Nie powstrzymało to MHRA przed wycofaniem produktu - po prostu pominęli ten problem, stwierdzając, że osoby, które miały historię alergii, nie powinny przyjmować szczepionki.
Nawet gdy wiedzieli - nanocząsteczki lipidowe ALC-0159 i ALC-0315 firmy Pfizer/BioNTech nigdy wcześniej nie były zawarte w żadnym licencjonowanym leku. ALC-0159 zawiera PEG (glikol polietylenowy), który jest wiadomo, że powoduje anafilaksję.
To jednoznaczne: anafilaksja była znanym zdarzeniem niepożądanym zagrażającym życiu, mniej więcej w tym samym czasie, gdy wydano zezwolenie na użycie awaryjne szczepionki Pfizer-BioNTech COVID-19. Jednak, ponieważ jest to „szczepionka do wstrzykiwania”, w jakiś sposób uzyskała bezpłatną przepustkę od wszystkich regulatorów leków, bez względu na to, ile gromadzą się potępiające dane, kiedy z drugiej strony syrop na kaszel lub kapsułka zostaje pilnie wycofana na podstawie „a bardzo rzadkie ryzyko anafilaksji”.
Opublikowane ponownie od autora Zastępki
Opublikowane pod a Creative Commons Uznanie autorstwa 4.0 Licencja międzynarodowa
W przypadku przedruków ustaw link kanoniczny z powrotem na oryginał Instytut Brownstone Artykuł i autor.









